식품의약품안전처(처장 오유경)는 의료제품 허가심사에 대한 투명성과 신뢰성을 강화하기 위해 12월 4주(12.19.~12.25.) 기간 의료제품 허가 현황을 제공한다고 밝혔다.
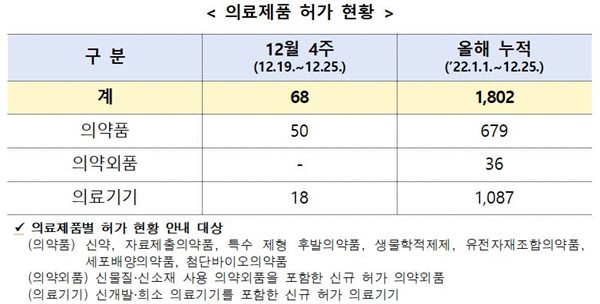
식약처(본부)는 12월 4주에 의료제품 총 68개 품목을 허가했다. (2022년 누적: 총 1,802개 품목)
12월 4주에 복잡성 복강 내 감염 등을 치료하는 신약 ‘자비쎄프타주2g/0.5g(세프타지딤/아비박탐)’(한국화이자제약, ’12.22)이 허가됐다.
| *세균 펩티도글리칸 세포벽 합성을 억제하여 세균 용해 및 세포사 유도(세프타지딤), 비(非)베타락탐계 베타락탐분해효소억제제로 항균력 유지(아비박탐) |
‘12월 4주 의료제품 허가 품목 리스트 의약품’ 현황에 따르면, 시타글리메트정50/1000밀리그램(동화약품), 시타콤비정50/850밀리그램(일동제약), 베프서방정(베포타스틴베실산염)(신풍제약), 타베온서방정(베포타스틴베실산염)(국제약품), 자비쎄프타주 2g/0.5g(세프타지딤/아비박탐)(한국화이자제약) 등이 포함됐다.
식약처는 “앞으로도 의료제품 허가 현황을 정례적으로 매주 제공하겠으며, 허가와 관련된 국민 관심이 높은 정보를 적극적으로 발굴해 공개·제공하는데 최선을 다하겠다”고 밝혔다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

