한국화이자제약 '리피토정10밀리그램', '카듀엣정5mg/20mg' 등 일부 품목이 '직접용기 병 목 테두리에 흠 발견 가능성 사유'로 회수를 진행한다.
일동제약 '벨빅정'(로카세린염산염수화물)의 경우 '안전성 속보 따른 영업자 회수 사유'로 회수 진행된다.
식품의약품안전처의 회수 현황 공지 뿐만 아니라, 한국화이자제약, 일동제약 등 해당 제약사들은 각사 홈페이지 공지를 통해 '리피토정10밀리그램'(한국화이자제약), '벨빅정'(벨빅정10mg·일동제약 회수안내문 포함) 등 해당 품목에 대해 회수 진행을 공지했다.
식품의약품안처 회수 현황(2월)<下 자료 참조>에 따르면, 일동제약 '벨빅엑스알정'(로카세린염산염수화물)의 경우, '안전성 속보 따른 영업자 회수' 사유로 회수진행(회수명령일자 2월 19일)된다.
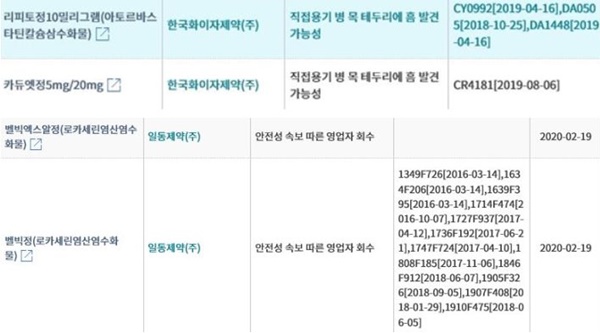
일동제약 '벨빅정'(로카세린염산염수화물)의 경우, '안전성 속보 따른 영업자 회수' 사유로 회수 진행된다.
회수명령일자는 2월 19일로 제조번호(제조일자)는 1634F206[2016-03-14],1639F395[2016-03-14],1714F474[2016-10-07],1727F937[2017-04-12], 1910F475[2018-06-05] 등이 해당된다.
앞서 식품의약품안전처는 지난 2월 14일 식욕억제 목적으로 사용하는 '로카세린' 성분의 향정신성의약품에 대해 판매중지 및 회수·폐기 계획을 알리고 의약전문가에게 처방·조제를 중단할 것을 요청했다고 발표했다. 대상은 '로카세린' 성분 함유 의약품인 일동제약의 '벨빅정' 및 '벨빅엑스알정' 2개 품목이다.
식약처는 지난 1월 16일 안전성 서한을 통해 국내 의약전문가 및 환자 등에게 '로카세린' 성분 의약품의 암 발생 가능성에 대해 처방 및 치료 시 이를 고려할 것을 권고한 바 있다.
미국 식품의약국은 '로카세린' 성분 의약품의 안전성 평가를 위한 임상시험<자료 참조>에서 위약 대비 암 발생 위험이 증가하는 것으로 나타나 제조사에 자발적 시장 철수를 요청했다.

식약처는 해당 의약품의 위해성(암 발생 위험 증가)이 유익성(체중조절 보조)을 상회하는 것으로 판단되어 판매중지 및 회수·폐기를 결정했다고 밝혔다.
이와 함께, 식약처 회수 현황(2월)에 따르면, 한국화이자제약 '리피토정10밀리그램'(아토르바스타틴칼슘삼수화물)의 경우 '직접용기 병 목 테두리에 흠 발견 가능성' 회수 사유로 회수 진행된다.
회수명령일자는 2월 12일로 제조번호(제조일자)는 CY0992[2019-04-16],DA0505[2018-10-25],DA1448[2019-04-16] 등이 해당된다.
한국화이자제약 '카듀엣정5mg/20mg'의 경우, '직접용기 병 목 테두리에 흠 발견 가능성' 사유로 회수 진행된다. 회수명령일자는 2월 12일로 제조번호(제조일자)는 CR4181[2019-08-06]이다. 회수명령일자는 2월 12일이다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

