한국얀센 'Golimumab(CNTO148)'의 경우, 중등증에서 중증의 활성 궤양성 대장염이 있는 소아 참가자에서 피하 투여된 인간 항-TNFα 단클론성 항체인 golimumab 치료의 유효성, 안전성 및 약동학을 평가하기 위한 제3상, 무작위 배정, 라벨-공개 임상시험 3상이 승인됐다.
종근당 'CKD-385'의 경우, 건강한 성인에서 CKD-385의 약동학적 특성 및 안전성을 평가하기 위한 무작위배정, 공개, 식후, 단회투여, 교차 임상시험 1상이 승인됐다.
대웅제약 'DWP14012정'의 경우, 미란성 위식도역류질환 환자에서 DWP14012의 유효성 및 안전성을 평가하기위한 다기관, 무작위배정, 이중눈가림, 활성대조, 평행군, 3상, 치료적 확증 임상시험 3상이 승인된 것으로 나타났다.
메디트리트저널이 식품의약품안전처의 최근 의약품 임상시험 승인현황<下 표 참조>을 확인한 결과, ▲한국얀센 'Golimumab(CNTO148)' 1상, ▲종근당 'CKD-385' 1상, ▲대웅제약 'DWP14012정' 3상, ▲바이엘코리아 'BAY 1093884' 2상, ▲JW중외제약 '리바로E정4/10mg(가칭) 1상 등으로 임상시험이 승인된 것으로 나타났다.
한국얀센 'Golimumab(CNTO148)'의 경우, 중등증에서 중증의 활성 궤양성 대장염이 있는 소아 참가자에서 피하 투여된 인간 항-TNFα 단클론성 항체인 golimumab 치료의 유효성, 안전성 및 약동학을 평가하기 위한 제3상, 무작위 배정, 라벨-공개 임상시험 3상이 승인됐다.
'Golimumab(CNTO148)' 임상 실시기관은 삼성서울병원, 서울대학교병원, 재단법인아산사회복지재단서울아산병, 연세대학교의과대학세브란스병원 등이다.
종근당 'CKD-385'의 경우, 건강한 성인에서 CKD-385의 약동학적 특성 및 안전성을 평가하기 위한 무작위배정, 공개, 식후, 단회투여, 교차 임상시험 1상이 승인됐다.
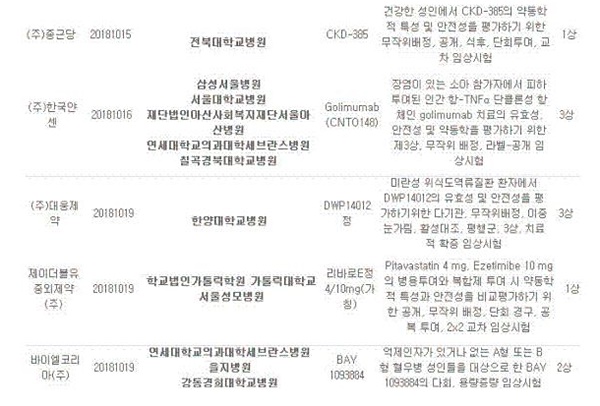
대웅제약 'DWP14012정'의 경우, 미란성 위식도역류질환 환자에서 DWP14012의 유효성 및 안전성을 평가하기위한 다기관, 무작위배정, 이중눈가림, 활성대조, 평행군, 3상, 치료적 확증 임상시험 3상이 승인됐다.
바이엘코리아 'BAY 1093884'의 경우, 억제인자가 있거나 없는 A형 또는 B형 혈우병 성인들을 대상으로 한 BAY 1093884의 다회, 용량증량 임상시험 2상이 승인된 것으로 나타났다.
제이더블유중외제약(JW중외제약) '리바로E정4/10mg(가칭)'의 경우, 건강한 자원자를 대상으로 Pitavastatin 4 mg, Ezetimibe 10 mg의 병용투여와 복합제 투여 시 약동학적 특성과 안전성을 비교평가하기 위한 공개, 무작위 배정, 단회 경구, 공복 투여, 2x2 교차 임상시험 1상이 승인됐다.
우정헌 기자 mtjpost@mtjpost.com
<저작권자 © 메디트리트저널(THE MEDI TRET JOURNAL), 무단 전재 및 재배포 금지>

