한국BMS제약의 '바라크루드정0.5mg', 한국화이자제약의 '비비안트정20mg' 등 다국적 제약사의 품목들이 수입업무정지 1개월의 처분을 받았다.
식품의약품안전처는 13일 한국BMS제약의 '바라크루드정0.5mg'과 한국화이자제약의 '비비안트정20mg' 등 품목들에 대해 수입 업무 정지 1개월의 행정처분<下 표 참조>을 내렸다고 밝혔다.
식약처에 따르면, 한국BMS제약(한국비엠에스제약) '바라크루드정0.5mg'(엔테카비르)은 해당 품목 수입업무정지 1개월의 처분을 받았다. 처분기간은 8월 20일부터 9월 19일까지이다.
식약처는 위반내용(약사법)에 대해 "의약품 '바라크루드정0.5밀리그램(엔테카비르)'를 제품표준서 중 용기 포장 견본에 기재된 포장단위(30정)와 다르게 정제가 부족한 제품을 수입·유통했다"고 밝혔다.
식약처는 "정상제품은 10정 단위 블리스터 3개가 2차 박스에 포장되어 총 30정이나 이중 10정 단위 한 개의 블리스터는 정제가 충전되어 있지 않은 공포켓이 포함됐다"고 밝혔다.
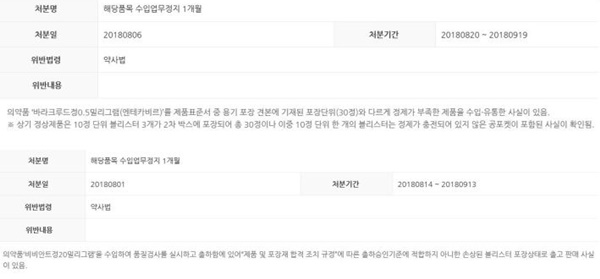
이와 함께, 한국화이자제약 '비비안트정20mg'은 해당품목 수입업무정지 1개월의 처분을 받았다. 처분기간은 8월 14일부터 9월 13일까지이다.
식약처는 위반내용(약사법)에 대해 "의약품 '비비안트정20밀리그램'을 수입해 품질검사를 실시하고 출하함에 있어 '제품 및 포장재 합격 조치 규정'에 따른 출하승인기준에 적합하지 아니한 손상된 블리스터 포장상태로 출고 판매 사실이 있다"고 밝혔다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

