식품의약품안전처(이의경 처장)는 전 세계적으로 코로나19 치료제 및 백신 개발이 활발히 진행되고 있는 가운데, 국내에서 개발되고 있는 치료제·백신의 임상시험 및 허가·심사 현황에 대한 정보를 제공한다고 1일 밝혔다.
식약처는 '계절 독감'과 '코로나19'의 동시 유행이 우려됨에 따라 이를 대비해 지난해보다 20% 증가한 약 3천만 명분의 계절 독감 백신 수급을 목표로 신속한 국가출하승인을 진행 중이라고 밝혔다.
◆치료제·백신 임상시험 승인 현황…GC녹십자 혈장분획치료제 2상 등 현재 진행 임상 총 17건= 현재 국내에서 승인된 임상시험은 총 22건(치료제 20건, 백신 2건)이다. 이 중 치료제 임상시험 5건이 종료되어 현재 진행 중인 임상시험은 총 17건(치료제 15건, 백신 2건)이다.
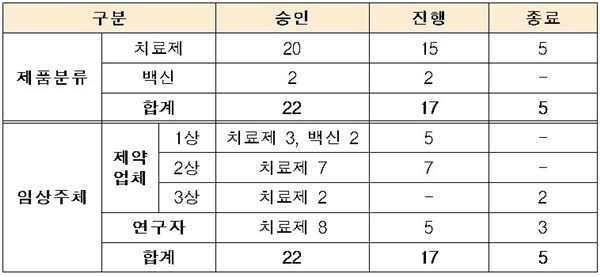
세부적으로는 제약업체가 진행하고 있는 임상시험은 12건이며, 연구자가 진행하는 임상시험은 5건이다. 제약업체가 진행하는 임상시험 중, 7건은 2상 임상(GC녹십자 혈장분획치료제 등), 5건은 1상 임상(셀트리온 항체치료제, DNA백신 등)이다.
◆치료제 개발 현황= 현재 국내에서 개발 중인 혈장분획치료제 및 항체치료제의 개발 진행 현황을 보면, 녹십자에서 개발 중인 혈장분획치료제는 지난 8월 20일 2상 임상시험을 승인받았으며, 삼성서울병원 등 6개 병원에서 9월부터 코로나19 증상 발현 7일 이내인 환자를 대상으로 임상시험을 실시할 예정이다.
셀트리온에서 개발 중인 중화항체치료제 신약(CT-P59)은 건강한 사람을 대상으로 한 임상 1상의 투약이 완료됐으며, 현재 2/3상 임상시험에 대한 계획이 심사 중에 있다.
한편, 셀트리온은 영국에서도 경증 환자에 대한 1상 임상시험을 승인받아 환자를 모집하고 있다.
◆계절독감·코로나19 동시 유행 대비 백신 신속 출하승인= 식약처는 '계절 독감'과 '코로나19'의 동시 유행이 우려됨에 따라 이를 대비해 지난해보다 20% 증가한 약 3천만 명분의 계절 독감 백신 수급을 목표로 신속한 국가출하승인을 진행 중이다. 이를 통해 무료 접종이 본격적으로 시작되는 9월 22일 이전까지 2천 6백만 명분 이상을 출하할 계획이다.
식약처는 "코로나19 치료제·백신의 임상시험 등 개발 동향을 지속적으로 모니터링하고, 이를 바탕으로 국내 도입을 위해 필요한 품목허가, 특례수입 등에 대한 사항을 지원해 우리 국민의 치료 기회를 보장할 수 있도록 최선을 다하겠다"고 밝혔다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

