녹십자 '아이비글로불린에스엔주5%' 등 면역글로불린 제제 '투여금지' 대상에 '면역글로불린에 과민반응 환자(특히 IgA에 항체가 있는 환자)'가 추가된다.
녹십자 '아이비글로불린에스엔주5%'·SK플라즈마 '리브감마에스앤주 허가사항 '용법 용량' 항목의 경우, "중증감염증에 항생물질 병용시: 1회 성인 2,500~5,000mg, 소아 체중 kg당 50~150mg을 점적정맥주사 또는 직접 정맥주사한다"는 내용이 허가 반영된다.
식품의약품안전처(처장 이의경, 이하 식약처)는 2일 녹십자 '아이비글로불린에스엔주5%'[말토즈 첨가 사람 면역글로불린(pH4.25)] 등 면역글로불린 제제에 대해 의약품 품목허가사항 변경지시<파일 참조>를 사전 예고했다. 허가사항 변경지시 예정일은 오는 7월 20일이다.
식약처는 녹십자 '아이비글로불린에스엔주5%'[말토즈 첨가 사람 면역글로불린(pH4.25)] 및 SK플라즈마 '리브감마에스앤주[말토즈첨가사람면역글로불린(pH4.25)]'에 대한 품목 허가갱신 결과 허가사항 변경지시(안)을 마련해 의견조회를 실시한 바 있다.
메디컬헤럴드가 식약처 '아이비글로불린에스엔주5%·리브감마에스앤주 허가사항 변경 대비표'<下 표 참조>를 확인한 결과, '투여 금지' 대상 항목에 "면역글로불린에 과민반응 환자(특히 IgA에 항체가 있는 환자)"가 추가된 것으로 나타났다.

허가사항 '용법 용량' 항목의 경우, "중증감염증에 항생물질 병용시 : 1회 성인 2,500~5,000mg, 소아 체중 kg당 50~150mg을 점적정맥주사 또는 직접 정맥주사한다"는 내용이 허가 반영된 것으로 나타났다.
식약처에 따르면, '아이비글로불린에스엔주5%'·'리브감마에스앤주' 허가사항 투여 금지 대상 항목에 "면역글로불린에 과민반응 환자(특히 IgA에 항체가 있는 환자)"가 추가됐다.
'아이비글로불린에스엔주5%'·'리브감마에스앤주 '용법 용량' 항목에 "저 및 무감마글로불린혈증: 1회 사람면역글로불린-지로서 체중 kg당 200~600mg을 3~4주 간격으로 점적정맥주사 또는 직접 정맥주사한다"는 내용이 허가 변경됐다.
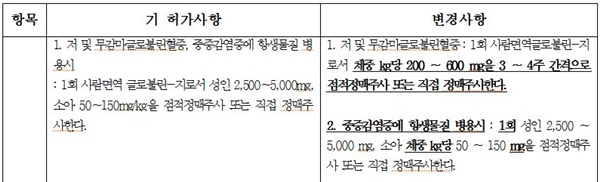
허가사항 '용법 용량' 항목에 "중증감염증에 항생물질 병용시 : 1회 성인 2,500~5,000mg, 소아 체중 kg당 50~150mg을 점적정맥주사 또는 직접 정맥주사한다"는 내용이 허가 반영됐다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

